Je ne suis pas parfait. Parfois, mes défauts rendent plus difficile la conception ou la cause de maladies héréditaires graves. Le PGT-A et le PGT-M sont des méthodes modernes de diagnostic embryonnaire utilisées pour détecter et éviter les défauts.
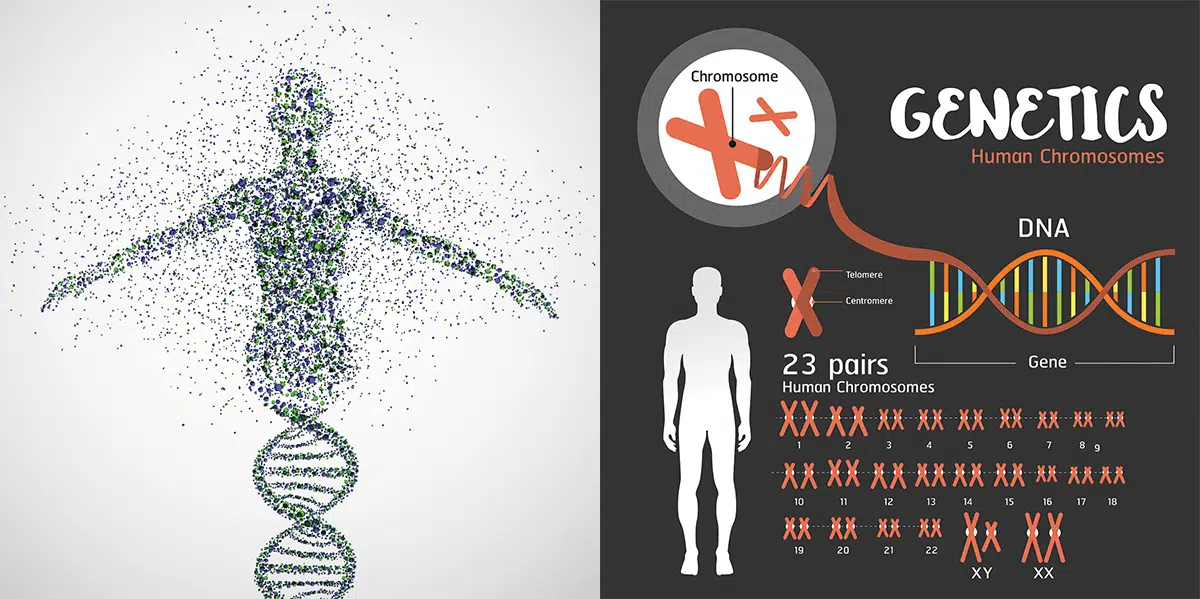
Je pense que vous avez une idée de qui je suis ou du moins vous avez entendu parler de moi. Selon toute vraisemblance, vous savez au moins que toutes les informations vous concernant sont emballées en moi. Vous savez peut-être aussi que je suis couramment présent sous forme de 46 chromosomes et d’innombrables, myriades de gènes chez l’homme. Dans vos gamètes, en revanche, il n’y a que la moitié de ce nombre pour mon autre moitié. Je suis votre ADN.
Sans trop m’avancer, il faut reconnaître mon originalité. Tout ce que vous êtes, tout ce qui vous rend unique, repose en moi. Grâce à moi, les orchidées fleurissent, les chiens courent dans les parcs, et quantité de bactéries se multiplient ou veillent sur votre intestin. Pourtant, malgré mes promesses, je accumule aussi des erreurs. Ces mutations imprévisibles et parfois dangereuses, ce sont mes défauts.
Défauts dans mon ensemble
Impossible d’ignorer les ratés généraux : les anomalies chromosomiques marquent souvent le destin d’une grossesse. Leur origine ? L’âge, surtout celui des ovules. Dès la naissance, la réserve d’ovocytes d’une femme s’épuise lentement. Avec l’arrivée des cycles, cette réduction s’accélère. À chaque ovulation, mon matériel génétique doit se diviser par deux pour fusionner, plus tard, avec celui d’un futur père. Et chaque année qui passe multiplie les chances de mauvaise division.
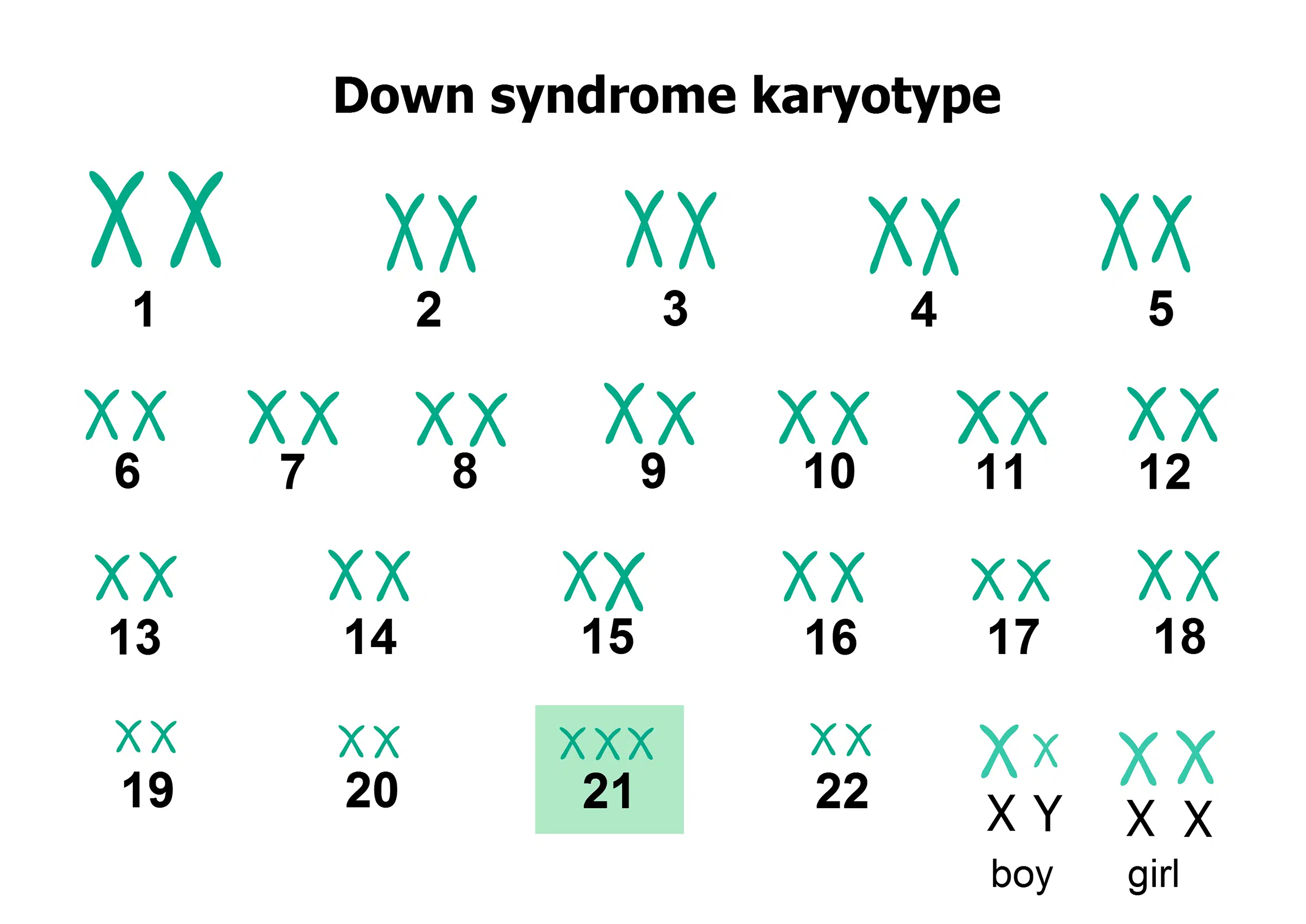
C’est ainsi qu’apparaît l’aneuploïdie, trouble du nombre de chromosomes. L’exemple le plus parlant : la trisomie 21, qui se traduit par la présence de trois chromosomes 21. Résultat, le syndrome de Down. Mais nulle région n’est épargnée, chaque chromosome peut être concerné.
Souvent, l’aneuploïdie interrompt la route bien avant la naissance. Le développement s’arrête, ou une fausse couche intervient sans prévenir. Plus le temps file, plus ces complications se multiplient, expliquant la chute du taux de grossesse spontanée ou assistée après 35 ans.
Des outils existent pour trier les embryons : à l’aide du PGT-A, il devient possible de repérer les aneuploïdies et de choisir ceux qui affichent un nombre de chromosomes conforme. Ce filtrage améliore les chances de succès d’une FIV, surtout après plusieurs tentatives infructueuses ou des pertes répétées.
Mais avant d’aborder comment se déroule ce diagnostic, il faut regarder de plus près un autre type d’erreurs.
Défauts de mes chromosomes
Parfois, c’est à l’intérieur d’un chromosome qu’une faille se glisse. Des micro-événements qui, la plupart du temps, sont neutralisés par un véritable service de réparation, protéines et enzymes agissent en gardiens vigilants. Malgré tout, certaines mutations leur échappent. Lorsqu’elles touchent les cellules destinées à la reproduction, ces défauts peuvent se transmettre à la génération suivante.
On retrouve dans cette catégorie la maladie de Huntington, plusieurs formes d’atrophies musculaires, ou l’INCL. Leur impact ? Radical, souvent dévastateur pour les patients et les familles.
Pour ces maladies précisément identifiées, le PGT-M offre une réponse ciblée : il permet de détecter les embryons porteurs d’un gène défectueux lorsque le risque est connu. Ce test est proposé quand deux parents savent qu’ils transmettent une anomalie génétique précise à leur descendance potentielle.
Venons-en à la méthode de détection proprement dite, celle qui scelle le destin de chaque embryon.
Mon parcours pour être diagnostiqué
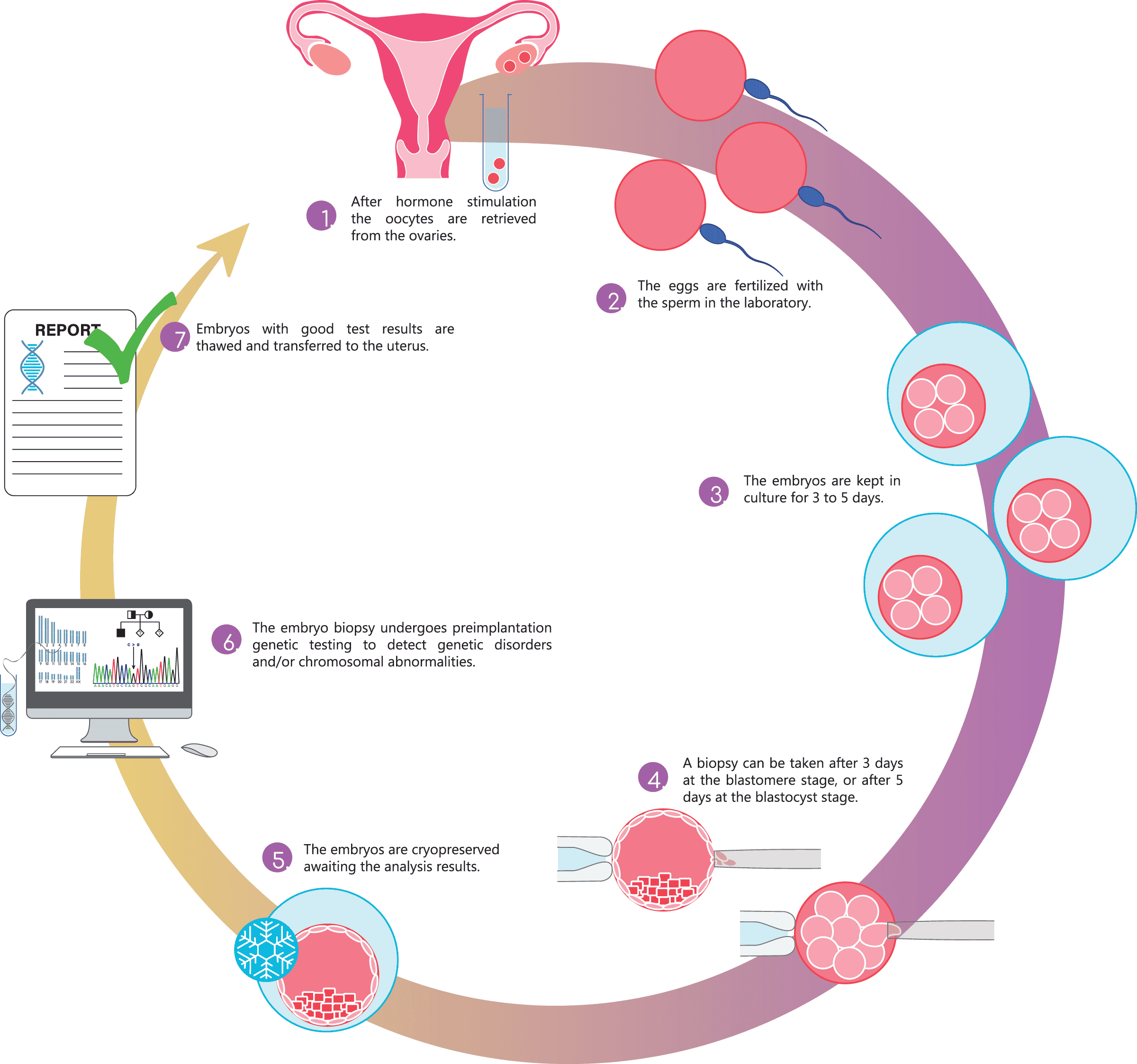
Autour du cinquième ou sixième jour après la fécondation in vitro, l’embryon compte une centaine de cellules. À ce stade, il est possible d’en prélever quelques-unes, rarement plus de 8, pour les analyser, sans réduire véritablement les chances de développement. Tout se passe sous contrôle permanent, grâce à des incubateurs robotisés et à une traçabilité minutieuse.
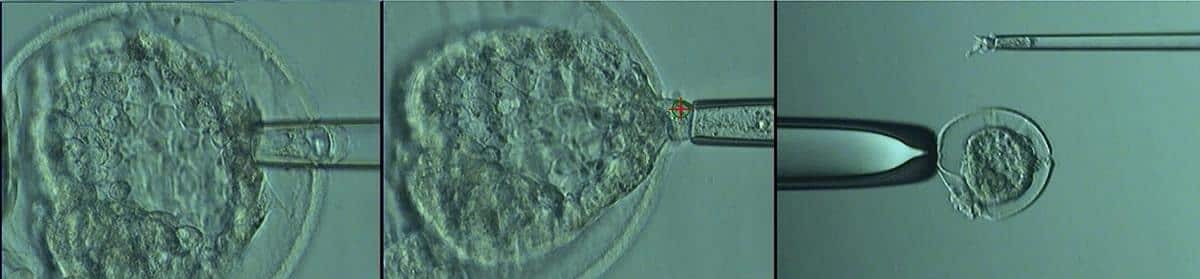
Pour illustrer, imaginez un spécialiste posté devant son microscope : il approche délicatement le premier embryon à l’aide d’un micro-manutentionnaire, perfore la zone de protection avec un laser d’une précision chirurgicale, puis aspire doucement les cellules sélectionnées. Ces précieuses cellules sont immédiatement placées dans des tubes étanches et refroidies à grande vitesse. Chaque embryon subit ce protocole, avant d’être soumis à la vitrification, une conservation par le froid extrême.
Puis, les échantillons partent vers des laboratoires spécialisés. Sur place, des experts scrutent chaque segment d’ADN comme un livre ouvert à la recherche de la moindre anomalie.
Lorsque les résultats arrivent, ce sont des moments chargés de tension. Tous les embryons ne sont pas toujours éligibles. Jusqu’à 40 ans, la probabilité qu’aucun ne convienne reste modérée, mais avec la quarantaine, le tri devient sévère.
Si un embryon sain est identifié, il sera délicatement décongelé puis transféré dans l’utérus. À partir de là, la suite s’écrit cellule après cellule, et moi, l’ADN, reprends les commandes, prêt à donner le meilleur. Reste à attendre que la biologie opère, parfois contre toute attente, jusqu’à ce premier cri longtemps espéré.