Je ne suis pas parfait. Parfois, mes défauts rendent plus difficile la conception ou la cause de maladies héréditaires graves. Le PGT-A et le PGT-M sont des méthodes modernes de diagnostic embryonnaire utilisées pour détecter et éviter les défauts.
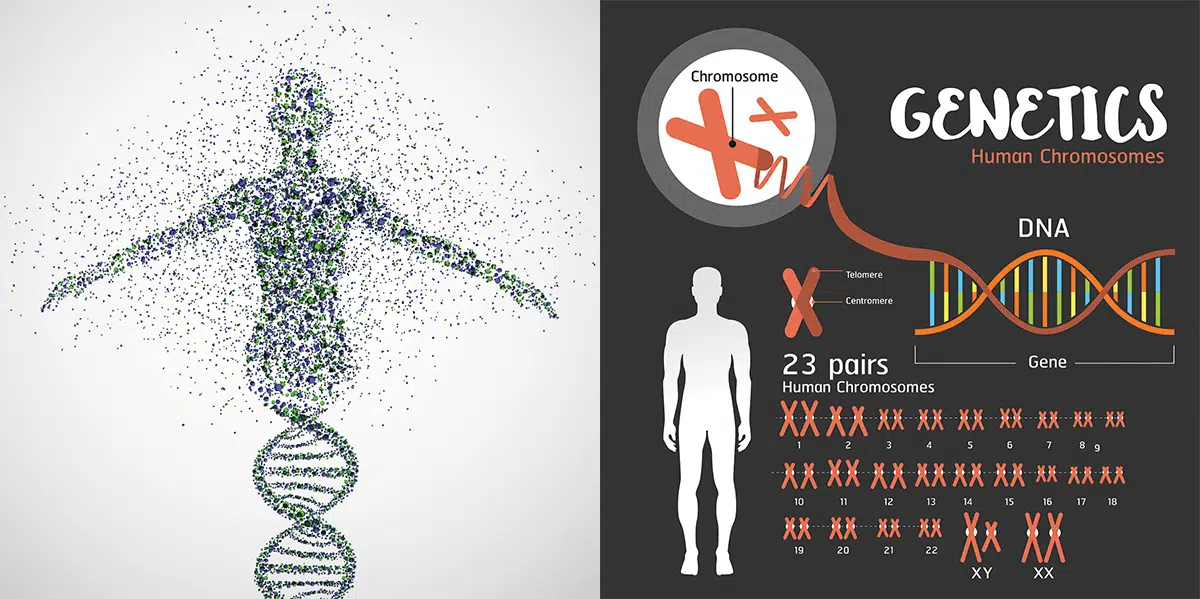
Je pense que vous avez une idée de qui je suis ou du moins vous avez entendu parler de moi. Selon toute vraisemblance, vous savez au moins que toutes les informations vous concernant sont emballées en moi. Vous savez peut-être aussi que je suis couramment présent sous forme de 46 chromosomes et d’innombrables, myriades de gènes chez l’homme. Dans vos gamètes, en revanche, il n’y a que la moitié de ce nombre pour mon autre moitié. Je suis votre ADN.
A voir aussi : Microsoft office 2016 activation avec clé
Sans trop m’affirmer, je peux dire que je suis assez incroyable. Je contiens des informations sur toute ma vie. Sans moi, vous n’auriez pas de plantes vertes sur le rebord de votre fenêtre et aucun chien ne serait assis autour de vous gratter. Sans moi, il n’y aurait pas de bactéries à l’origine d’une gamme de maladies ou, d’autre part, favorisent votre bien-être. Je ne suis pas parfait de toute façon. En moi, de nombreuses mutations sont nocives pour les créatures vivantes. J’appelle ça mes défauts.
Plan de l'article
Défauts dans mon ensemble
Le défaut le plus significatif de la grossesse concerne les anomalies chromosomiques. Celles-ci, à leur tour, sont très associées à l’âge de la femme et de ses ovules. Peut-être savez-vous que la réserve d’œufs de la femme existe déjà à sa naissance. La réserve commence à se rétrécir d’elle-même immédiatement après la naissance et, de plus, la quantité d’ovocytes diminue au début des menstruations de la femme. Pendant la menstruation, un ovule mûrit généralement dans les ovaires. C’est alors que mon nombre a diminué de moitié pour qu’il y ait de la place pour 23 autres chromosomes provenant du sperme. Au fur et à mesure que la femme vieillit, malheureusement, la probabilité que je ne diminue pas de moitié augmente normalement.
Lire également : CanMP : la plateforme de gestion administrative simplifiée
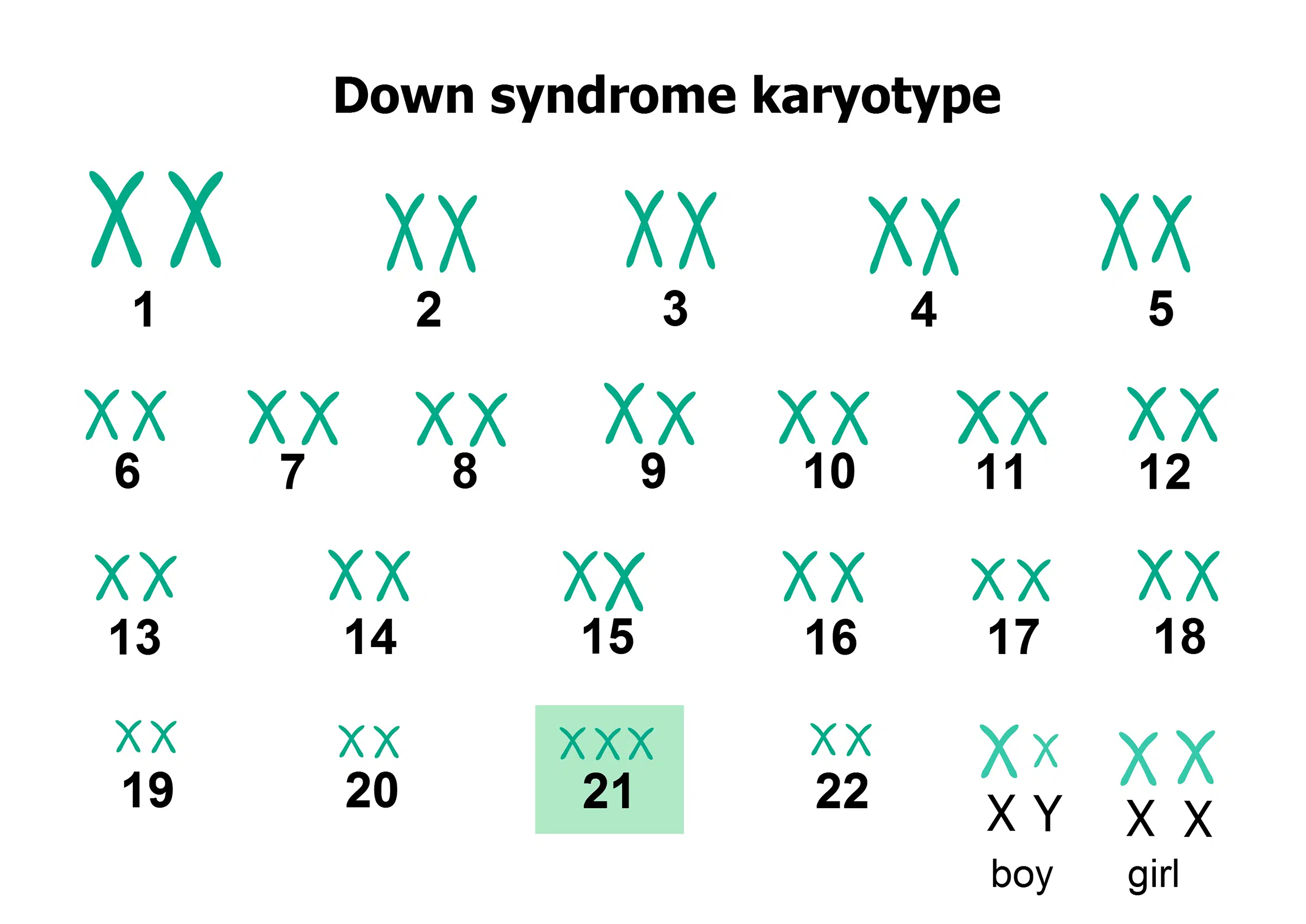
Cela conduit à une aneuploïdie, ce qui signifie que l’embryon a un nombre anormal de mes chromosomes. Le cas le plus célèbre est qu’il existe un chromosome 21 supplémentaire, la trisomie, qui provoque le syndrome de Down. Ensuite, il n’y a pas deux, mais trois morceaux de chromosome 21. Cependant, l’aneuploïdie peut toucher n’importe quel chromosome.
Dans l’aneuploïdie, il est plus fréquent que le développement de l’embryon s’arrête ou que la grossesse se termine par une fausse couche précoce que le bébé né. C’est la principale raison pour laquelle la fécondation spontanée et assistée est plus difficile à mesure que l’on vieillit.
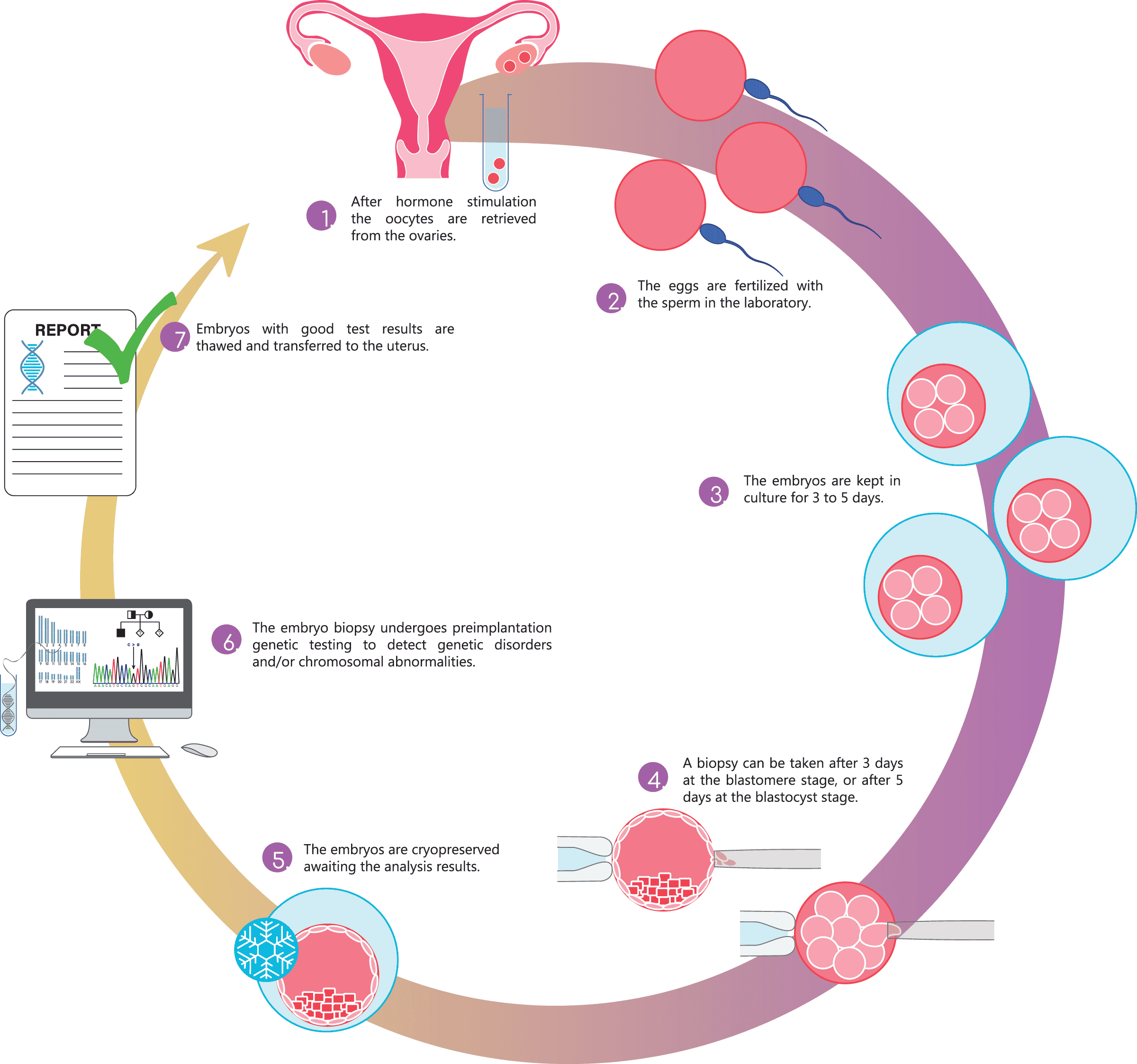
La bonne nouvelle est que les embryons aneuploïdes peuvent être identifiés. Cela se produit avec une méthode d’embryodiagonostique appelée PGT-A (Preimplantation Genetic Testing for Aneuploïdy). L’ancien terme PGS est finalement incliné). Lorsque, dans le contexte d’une fécondation par éprouvette, des embryons ont un nombre normal de mes chromosomes transférés vers l’utérus, la probabilité que la femme tombe enceinte est significativement plus grande que si les chromosomes ne sont pas examinés. En plus facteur d’âge, il est sage de faire du PGT-A aussi si la femme a subi plusieurs fausses couches ou a échoué.
Mon parcours pour être diagnostiqué est intéressant, mais avant de vous en parler, je voudrais vous en parler peu sur un autre de mes défauts.
Défauts de mes chromosomes
Un autre défaut se produit à l’intérieur de l’un de mes chromosomes. En fait, de telles erreurs se produisent en moi tout le temps. Cependant, j’ai de la chance, car j’ai de fidèles troupes auxiliaires autour de moi qui identifient et réparent la plupart des défauts. Je ne ferais pas sans eux.
Malheureusement, l’identification et la réparation ne fonctionnent pas toujours correctement. Les mutations peuvent alors causer de nombreuses maladies différentes. Si le défaut est détecté dans les cellules germinales, il peut arriver que la maladie soit héritée par les générations suivantes. Parmi ces maladies, citons la maladie de Huntington, de nombreuses atrophies musculaires et l’INCL, entre autres.
Tous ces éléments sont sérieux, maladies héréditaires incurables qui ont un impact très important sur la vie humaine. En ce qui concerne l’ancien défaut, des diagnostics embryonnaires connus dans ce cas sous le nom de PGT-M (Preimplantation Genetic Testing for Monogenic Diseases) peuvent également être utilisés. L’ancien terme PGD est finalement incliné). Grâce à cette méthode, les embryons dont les gènes sont malades peuvent être identifiés presque sans exception. Le test peut être effectué s’il est connu que la paire est porteuse d’un défaut génétique à l’origine d’une maladie particulière.
Maintenant, pour le voyage dont j’ai promis de vous parler.
Mon parcours pour être diagnostiqué
Image du mode : Je suis dans un laboratoire à l’intérieur des cellules d’embryons au stade blastocyste. À ce stade, les jours 5-6, il y a une centaine de cellules, ce qui est bien. Ensuite, environ 5 à 8 cellules peuvent être retirées pour un diagnostic embryonnaire et les embryons sont malgré cela viables. Les embryons ont pu se développer dans des conditions très stables, car depuis leur conception, ils ont été préservés en culture. et dispositif de suivi pour embryons connus sous le nom d’EmbryoScope.
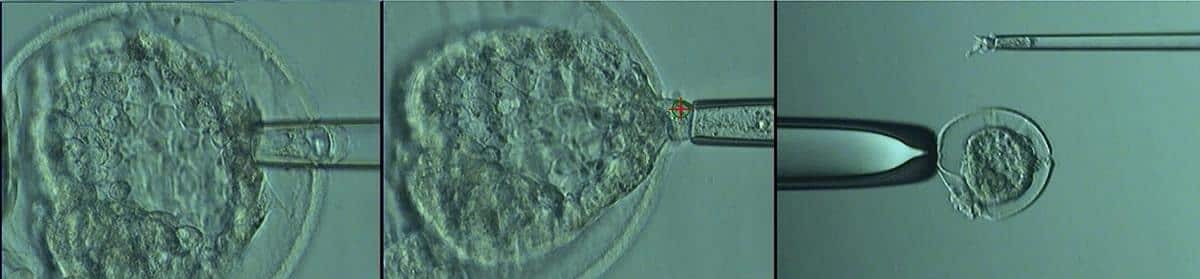
Bientôt, Peter Bredbacka, spécialiste de la PGT d’Ovumia, commence à effectuer une biopsie à partir des cellules à l’intérieur desquelles je me trouve (en savoir plus sur Peter dans notre texte de blog suivant). Peter microscope le premier embryon et l’attrape avec le capillaire micro-manipulateur qui suce faiblement et méfiablement. Quand Peter fait ressortir le laser, je ne touche pas une minute. Je sais que je suis entre de bonnes mains. Peter est un expert possédant une vaste expérience. Peter fait un petit trou avec le laser dans la coquille de l’embryon, la zone pellucide dite (voir la série d’images ci-dessous). Ensuite, à l’aide d’un autre capillaire, il aspire un nombre nécessaire de cellules par le trou et place les cellules au fond d’un petit tube à essai. Le tuyau est immédiatement placé dans l’armoire congélateur. Peter fait de même avec tous les embryons. Enfin, les embryons sont gelés par vitrification et placés dans un récipient d’azote liquide où ils attendent les résultats de l’analyse.
Les tubes contenant des cellules sont envoyés comme transport de refroidissement vers différentes parties de l’Europe pour être testés dans des laboratoires d’essai en fonction de ce que l’on veut analyser. Au laboratoire d’essais, je suis enfin examiné par des experts en génétique.
Une fois les résultats terminés, Peter les explique aux clients. Il me dit combien d’embryons sont normaux et lesquels peuvent être transférés. Malheureusement, le résultat montre parfois qu’aucun embryon ne peut être utilisé. Chez les femmes de moins de 40 ans, c’est rarement le cas, mais le risque augmente avec les années.
Enfin, lorsque l’embryon fraîchement déclaré a été décongelé et retourné dans l’utérus, c’est moi qui prends le relais. Je donne les ordres nécessaires et j’espère que le fruit de mon travail sera mûr dans neuf mois.