Certains remarquent à peine qu’ils ont eu la maladie, d’autres présentent des symptômes particuliers. Un autre est tellement malade qu’il doit recevoir des soins intensifs, et certains s’en vont. Pourquoi le covid-19 frappe-t-il si différent et que se passe-t-il dans le corps lorsque nous sommes infectés par le virus ? Visualisation des virus SARS-COV-2 par microscopering. Photo : istock.com/narvikk
A lire également : Sécurité des opérations bancaires en ligne : ce qu'il faut savoir avant de se lancer !
Les virus. On les décrit parfois comme de simples paquets de gènes enveloppés dans une armure de protéines. Leur stratégie : infiltrer nos cellules en accrochant leurs protéines à des récepteurs précis, puis y injecter leur matériel génétique, à l’abri des attaques extérieures.
Pour le SARS-CoV-2, responsable de la pandémie de covid-19, cette manœuvre commence par la fixation à un récepteur bien connu : l’ACE2. Guidé par une protéine de pointe, le virus s’arrime, puis force la porte cellulaire. Une fois à l’intérieur, c’est un véritable piratage : le virus détourne la machinerie de la cellule pour se multiplier et libérer de nouvelles particules virales, prêtes à infecter les cellules voisines. Marianne Jansson, professeure agrégée de virologie à l’Université de Lund, explique que ce mécanisme, implacable, fait du SARS-CoV-2 un adversaire redoutable. Elle participe d’ailleurs à la création d’un centre de recherche sur les virus à Lund, prévu pour l’automne.
A lire en complément : Protection antivirus pour téléphones portables : tout ce qu'il faut savoir
Quand les premières cellules du corps sont contaminées, la riposte commence. La défense immunitaire innée se met en route dès que le génome viral pénètre dans la cellule. Rapidement, des molécules appelées interférons sont produites, pour alerter les cellules alentours et tenter de freiner la propagation.
Mais cette protection de première ligne n’est pas infaillible. Si elle l’était, les infections virales ne seraient qu’un mauvais souvenir depuis longtemps.
Anticorps, lymphocytes : la riposte sur-mesure
Ce que chacun espère après un épisode de covid-19, c’est la fabrication d’anticorps. Cette défense, plus sophistiquée, fait appel à l’immunité acquise avec ses deux piliers : les lymphocytes B et T. Mais ces cellules spécialisées ont besoin d’être activées : il faut d’abord leur présenter le virus, ou plutôt des fragments de ses protéines, pour qu’elles entrent en action. Ce délai explique pourquoi la réponse immunitaire spécifique arrive plus tard.
La scène se déroule ainsi : des cellules « présentatrices d’antigènes » digèrent des résidus de virus ou de cellules mortes, puis exhibent ces fragments à la surface. Les lymphocytes T auxiliaires les reconnaissent, envoient le signal aux lymphocytes B, qui commencent alors à fabriquer des anticorps dirigés contre le pathogène. Les lymphocytes T tueurs, eux, partent à la chasse aux cellules déjà infectées.
Suite à cette bataille, des cellules mémoire B et T persistent dans l’organisme. Leur rôle : rester en veille, parfois des années durant, prêtes à intervenir rapidement au moindre nouveau contact avec le même virus. C’est le fondement même de l’immunité durable.
Une étude récente le montre : une réponse immunitaire robuste au covid-19 reste détectable chez la majorité des personnes, même huit mois après l’infection. Les chercheurs ont analysé, entre autres, les cellules mémoire, et ont constaté que les cellules B étaient toujours là, capables de se réactiver en cas de nouvelle exposition et d’offrir une protection contre une nouvelle attaque.
Vieillir, c’est aussi affronter un système immunitaire fatigué
Le risque de développer une forme grave de covid-19 croît avec l’âge. Rien de surprenant à cela : de nombreuses infections, banales chez l’enfant, deviennent plus sérieuses à l’âge adulte. Le système immunitaire vieillit, lui aussi, et d’autres maladies s’ajoutent, telles que des pathologies pulmonaires, cardiaques ou rénales, compliquant le tableau.
Marianne Jansson précise que la capacité à bien démarrer la réponse immunitaire innée semble déterminante pour l’issue face au SARS-CoV-2. Si cette première réaction, notamment la production d’interféron, est trop faible, en raison de facteurs génétiques ou d’autres variations, le risque de complications augmente.
Des différences entre hommes et femmes
Nos défenses immunitaires varient d’un individu à l’autre, mais aussi selon le sexe. Les femmes sont plus sujettes aux maladies auto-immunes, quand l’organisme s’attaque à lui-même. Mais dans le contexte des infections, cette activité immunitaire accrue peut se révéler bénéfique. Pourtant, les hommes paient un tribut plus lourd face au covid-19 : ils sont environ trois fois plus nombreux à nécessiter des soins intensifs.
Les raisons sont multiples. Les hormones sexuelles influencent la réponse immunitaire différemment chez les hommes et les femmes. Certaines études suggèrent même que les hormones pourraient jouer un rôle sur l’expression des récepteurs du covid-19. Des recherches restent à mener pour démêler l’impact exact de ces facteurs.
L’immunité croisée : un atout caché
Autre paramètre : la mémoire immunitaire acquise lors d’infections antérieures par des virus similaires. Qui a déjà affronté un coronavirus proche du covid-19 peut garder en réserve des cellules mémoire, prêtes à réagir dès la première alerte. Cela peut permettre de lutter plus tôt, grâce à la mobilisation rapide d’anticorps et de lymphocytes T.
Un exemple marquant : certaines personnes âgées sont mieux protégées contre de nouvelles souches de grippe parce qu’elles ont déjà rencontré des variantes anciennes, inconnues des plus jeunes. Des recherches publiées indiquent aussi que les coronavirus responsables de rhumes communs pourraient induire une immunité partielle contre le covid-19.
Cette protection croisée semble surtout bénéficier aux jeunes, qui ont souvent été exposés récemment à ces virus. Par ailleurs, un individu réinfecté par le covid-19 fait rarement une forme aussi grave la seconde fois. Cela montre que la mémoire immunitaire, anticorps, lymphocytes T, bien que n’empêchant pas toujours la réinfection, aide à prévenir les formes sévères. On peut aussi supposer que des infections répétées par d’autres virus du rhume, en stimulant la production d’interféron, influencent la dynamique du covid-19.
Quantité de virus, mutations : des facteurs aggravants
Pourquoi certains passent sous les radars des tests d’anticorps malgré une infection légère ou silencieuse ? Parce que le virus peut déclencher une réponse immunitaire basée sur les lymphocytes T, sans forcément stimuler la production d’anticorps détectables. Cette immunité cellulaire peut suffire à contrôler l’infection et laisser une trace durable dans l’organisme.
La dose de virus reçue au moment de la contamination compte également. Une exposition massive ou répétée peut augmenter la gravité de la maladie. Par ailleurs, certaines variantes du covid-19, plus aptes à infecter, pourraient s’expliquer par une meilleure affinité avec les récepteurs cellulaires et une présence prolongée du virus dans les voies respiratoires. Les connaissances progressent, mais bien des aspects restent à explorer.
Hyperinflammation : quand la défense s’emballe
Chez une minorité, covid-19 entraîne une réaction excessive du système immunitaire. Cette surréaction, dite hyperinflammation, provoque la libération massive de molécules pro-inflammatoires, pouvant conduire à des défaillances graves, en particulier au niveau des poumons. Désormais, un traitement à base de cortisone permet de modérer cette cascade inflammatoire et de limiter les dégâts.
Chez les enfants, la très grande majorité traverse le covid-19 sans complication. Pourtant, quelques-uns développent, des semaines après l’infection, un syndrome inflammatoire multisystémique (MIS-C), sorte de réaction auto-immune dont les causes restent à élucider.
La recherche sur le covid-19 reste intense. Comprendre pourquoi certains subissent des formes sévères ou prolongées du virus demeure une priorité. Le développement de nouveaux médicaments antiviraux, capables de freiner l’évolution de la maladie et de limiter la transmission, est également en ligne de mire.
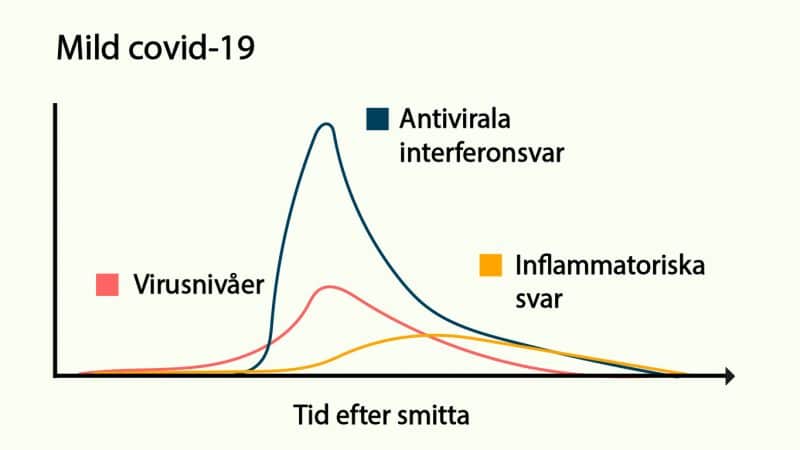
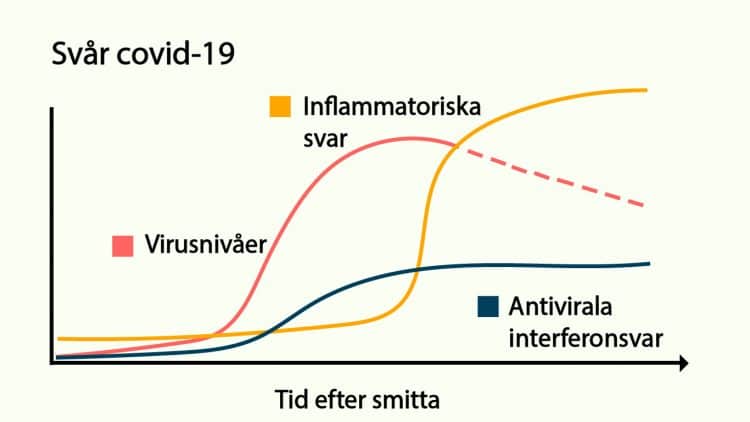
Les graphiques ci-dessous illustrent deux trajectoires possibles de la réponse immunitaire antivirale après infection par le SARS-CoV-2 : un scénario de covid-19 léger, fréquent chez les jeunes, et un autre sévère, plus courant chez les personnes âgées. Quand la réponse innée, notamment l’interféron, est rapide et efficace, la multiplication virale et l’inflammation restent sous contrôle. À l’inverse, une réponse tardive ou insuffisante laisse le champ libre au virus, aboutissant à une inflammation massive et à une maladie grave. Ces schémas sont inspirés des travaux de Feuillet et collègues (Trends in Immunology).
Le second graphique donne un aperçu du déroulement habituel d’une infection virale ordinaire.
Faits vérifiés par Marianne Jansson
Par : TOVE SMEDS